
UN IVE RS ID AD E JOSÉ D O ROSÁ R IO VE LLA NO – 2018
Características gerais dos
compostos orgânicos
Aluna: Gabriela A bra ntes Ni cáci o
Matr íc ula: 202411151
D i sci pli na : Q u ímica Orgâ ni ca
Be lo Hori zo nte, 05 de o ut ubro de 20 18

C aracter ística s gerai s dos compostos o rgâni cos
F orças Intermoleculares na Quí mica Org ânica
As forças i nter mole c ula res ma ntêm d uas o u mai s moléc u las unid as. E stas forças
correspondem a li gaçõe s q uímicas capa ze s u ni r o u repe li r as mo léc ulas de um composto , q ue
pode m ser mai s ou me no s forte s co nforme a polari dade da s moléc ulas . As forças
i ntermo lec ula res geram no s compostos q uímico s es tado s f ísicos di fere ntes .
Existem t rês ti p os de forças intermo lec ulares , que são: dip olo permane n te, di po lo i nd u zi do e
li gaçõe s de hi d rog ê ni o.
D ipo lo p ermanente
Essa força po ssui i ntensi da de médi a e ocorre somente em moléc u las p olares, o nde os elétro ns
estão di strib uídos d e forma a ssi mét ri ca, o nde uma parte da mo léc ula p oss ui mai o r de nsi dad e
eletrô ni ca.
Qua ndo a moléc ula é di a tômica , o elemento mai s eletro negativo atrai os elétro ns da liga ção e
força um d i polo elé trico . A ssi m, a pa rte po si ti va a t rai a par te neg ati va de o u tra moléc ula e
assi m sucessi vame nte.
D ipo lo in du z ido
A força de di polo i nduzid o é a de menor i nte nsi da de e ocorre em mo léc ulas pola res e a polares
No enta n to, q uando essa s moléc ulas (ou á tomos – gase s nobres) se aproxi mam uma das
out ras, pode m o correr de for mações na s nuve ns ele trô nica s, po i s há atrações e repulsõe s ent re
os elétro ns e o s núcleo s dos átomos . A deformação é ap enas tempo rá ria, mas forma regiõ es
do á tomo ou da mo lécu la q ue fi cam com mai or q uanti da de d e elétro ns, p or tanto, são fo rmados
di polos i nsta ntâ ne os.
O d i polo i ns tan tâ neo ao se apro xi mar de o u tras mo léc ulas pod e i nd u zi r a o utra moléc u la a
também se polari zar e assi m ocor rem forças a trati vas - fo rças de dip olo i nd u zi do.
Ligaçõ es de H id rogên io
A li gaçã o de hi drogênio é a força i ntermolec ular mai s i nte nsa , po i s exi ste u ma grande di fere nça
de e letro ne gativi da de en tre os eleme ntos . E sta li gaçã o oco rre em moléc ulas p olares q ue têm o
hi drogênio uni do a e leme ntos com vo l ume a tô mico bai xo e e letro neg ati vos co mo o hid rog ê ni o,
fl úo r , o xi g êni o e ni t rogênio .
D e um lad o, um áto mo m ui to p osi ti vo e, do o utro, um á tomo m ui to nega ti vo. Isto fa z co m q ue a
atração e ntre estes á tomos se ja mui to for te. P or i sso, e m gera l são só lido s ou l íq ui dos .
Entre a s mo léculas de á gua o corre este tipo de força i ntermo lec ular . O nd e, o o xig êni o p ossui
carga parcia l negati va e o s hi drogênio s possue m carga pa rci al posi ti va . E ntão, um hi drogênio
de uma mo lécu la é atra ído pelo o xi g êni o d e out ra moléc ula e assi m por di a nte, forma ndo
li gaçõe s de hi drogê nio .
Uma co nse q uênci a das po ntes de hi drogê ni o que e xi ste m na ág ua é a s ua e le vada te nsão
supe rfici al, ond e as moléc u las q ue estão no i nteri or d o l íq ui do atraem e são a tra ídas por todas
as moléc ulas vi zi n has, de tal modo q ue as essas forças se eq ui libram . Já as mo lécu las d a
supe rf ície só são a tra ídas pelas moléc ulas de b ai xo e do s lad os. E ntão , essas moléc ulas se

atraem mai s for teme nte e cri am uma pe l íc ula na s up er f íci e d a ág ua q ue e xp li ca a lg uns
fenôme no s , como o fato de alg uns i nse tos ca mi nhare m sobre a ág ua, e a forma esfé rica d as
gotas de ág ua .
E stru tu ra e P ropried ade s d o átomo de ca rbon o
O átomo de ca rbo no
O carbono está locali zado no grupo 1 4 (fam íli a IV A) e p ossui se i s elétrons, sendo qua tro de stes
locali zad os e m s ua camada de va lê nci a. P orta nto , o carbono é te tra vale nte e reali za qua t ro
li gaçõe s covale ntes para adqui ri r s ua estab i li dade química . E le p ode rea li zar li gaçã o com
out ros átomos de ca rbo no e for mar vário s ti pos de cade i as. O á tomo de ca rbono se li ga a
eleme ntos co muns em co mpostos o rgâni cos, como o hi d rog ê ni o, o xi gênio , nitrogê nio , e nxo fre e
halogê ni o s (Cl , Br , F, I).
Es trutura
O ca rbo no for ma es tr ut uras te traédrica s. O nde o átomo d e ca rbono locali za -se no ce ntro d e
tetraedros reg ulares e se us ligan tes oc upam a s e xt remi da des. As ligaçõ es forma m e nt re si
âng ulos de 109,5º q ue é a a ngulação mais estável p ara estr ut uras co nte nd o carbono , o nd e, em
cade i as cícli cas, a s liga ções en tre carbo nos a prese ntam â ng ulos i nferi ores a 1 09º5, o q ue as
tor nam mais fraca s .
Tipos de ligação
O carbono rea li za li gações do tip o cova le nte com ame tai s (C , O, S , C l, Br, I, F, etc .) e
hi drogênio . E stas li gaçõe s pod em se r d o ti po σ o u π d e acordo co m o entrosamento d e orbi tai s
na rea li za ção da li gação .
Qua ndo essas li gaçõ es ocorrem p or i nterpe ne tração de o rbi tais no mesmo ei xo de li gação , a
li gação será do tipo σ ; quando a li gaçã o for rea li zada p or i nteração de orbi tai s paral e los ent re
si , a lig ação rea li zada se rá do tipo π.
A regra pa ra p re ver se a li gação do carbo no será do ti p o σ o u π é:
• Li ga ções si mples são do ti po σ ;
• E m li ga ções dup las, uma das li ga ções é do tipo σ e a adi ci onal é do ti po π ;
• No caso de liga ção tri p la , uma da s li gaçõe s é do ti po σ e d uas são do ti po π;
H ibrid iz a ção
Hi bridi za ção é a uni ão de orbi tais atômico s i nco mpletos. Um orbi tal é c lassi ficad o co mo
i ncomple to qua ndo ele apresenta apena s um e létro n em seu i nterior ao em ve z de doi s. A
hi bri di zação é um fe nôme no na t ural q ue ocorre co m a lg u ns eleme ntos q u ími cos, como o
Fósforo, o E nxo fre e o C arbo no . A hi bri di zação do C arbo no permi te q ue os á tomos desse
eleme nto seja m capa zes de reali za r q ua tro li gaçõe s quími cas, com i sto , o ca rbo no só reali za
qua tro li gaçõ es ap ós so frer o fe nôme no da hi bri di zação .
C lass ificaçõ es d o Carbo no
O carbo no po de se r c lassi fica do d e acordo co m o núme ro de ligaçõ es que rea liza com o ut ros
átomos de carbo no. A s c lassi ficaçõe s são reali zadas da seg uin te ma nei ra:

• C arbono pri mári o: lig a -se a um á tomo de ca rbono ;
• C arbono sec undário: li ga -se a dois átomos de carbo no ;
• C arbono te rciá ri o: li ga -se a três átomos de carbo no ;
• C arbono q ua ter nári o: se li ga a q uatro átomos de carbo no .
Po stulad o de C ou pe r-K eku lé
Os est udo s refere ntes a estr ut u ra do ca rbo no fo ram de no mi nad os post ulados d e C ouper -
Ke kulé q ue est uda m o compor tame nto q uímico do carbo no , eles são s ubdi vi di do s em três:
1º po stulad o : Tetra va lência co nsta nte . O á tomo de carbono é tetra va le nte, essa p roprie dade
permi te q ue esse elemento e stabe leça quat ro ligaçõ es covale ntes, o nde ele po ssui doi s pares
de elé tro ns di sp onívei s.
2º po stulad o : A s quatro va lê nci as do ca rbo no são i guai s. P ortanto, um átomo po de se ligar a
qua lq uer um dos qua tro carbo nos di sp oníve i s q ue i rá for mar o mesmo composto .
3º p ostulad o : E ncad eamento co nsta nte. Átomos de carbono lig am-se di retame nte en tre si,
forma ndo cad ei as ca rbô ni cas. Essa propri ed ade também é o bserva da no ni trogêni o, e n xofre ,
fósforo e o xi g êni o. Mas , no ca rbono e ssa cap aci dade de formar q uatro li gaçõ es é mai s
pronunci ad a do que nos o utros compos tos, po r i sso é p ossíve l o bser var uma g ra nd e va ried ade
de compostos orgâ ni co s e cadei as e xte nsas de carbo no.
R eg ras g erais d e n omenc latura
A nomenc lat ura IUPA C refe re-se ao estab eleci me nto d e regras p ara a e scri ta d os nomes dos
compostos q ue são o fi ci almente acei tos e m todo o m u ndo.
R eg ras:
A nomenc lat ura de C ompostos Orgâ ni cos de cadeia no rmal e não aromáti cos segue o seguin te
esquema:
Prefi xo + Infi xo + S ufi xo
Ta bela com os respecti vos p refi xos e m relação a q ua ntida de de carbonos presente na ca dei a
princip al:
Qua ntidad e de
C arbon os
Prefixos
1
Met
2
Et
3
Prop
4
B ut
5
Pe nt
6
H ex
7
H ept
8
Oct
9
N on
10
D ec
11
U nd ec
12
D od ec

13
Tride c
14
Tetradec
15
Pe ntade c
16
H exadec
17
H eptade c
18
Octadec
19
N on ade c
20
Eicos
21
H on eico s
22
D oco s
23
Trico s
24
Tetracos
25
Pe ntaco s
30
Triaco nt
40
Tetracon t
50
Pe ntaco nt
60
H exac on t
70
H eptaco nt
N omenc latura de C ompo stos co m C ade ia Ramificad a
1º Escol ha da C ade i a P rinci p al
A cadei a pri nci p al é aq uela que aprese nta as seg ui ntes caracte r ís ticas:
Po ssui o gr upo f unci o nal ;
C onsta daq ue la com o maio r n úmero po ss íve l de i nsat uraçõ es;
Po ssui a seq uênci a mais lo ng a de á tomos de carbo no li g ados e nt re si .
Observações:
C aso a cadei a pri ncip al ofereça mai s de u ma p ossi bi li da de de escolha , de ve -se opta r por
aquela que for ne cer o mai o r número de rami ficaçõ es.
Qua ndo a cade i a é mista de ve mos co nsid erar co mo cadei a princi p al a ca dei a fec hada
(alic ícli ca) ou a par te aro máti ca .
R amific açõ es imp ortan tes (R ad icais):
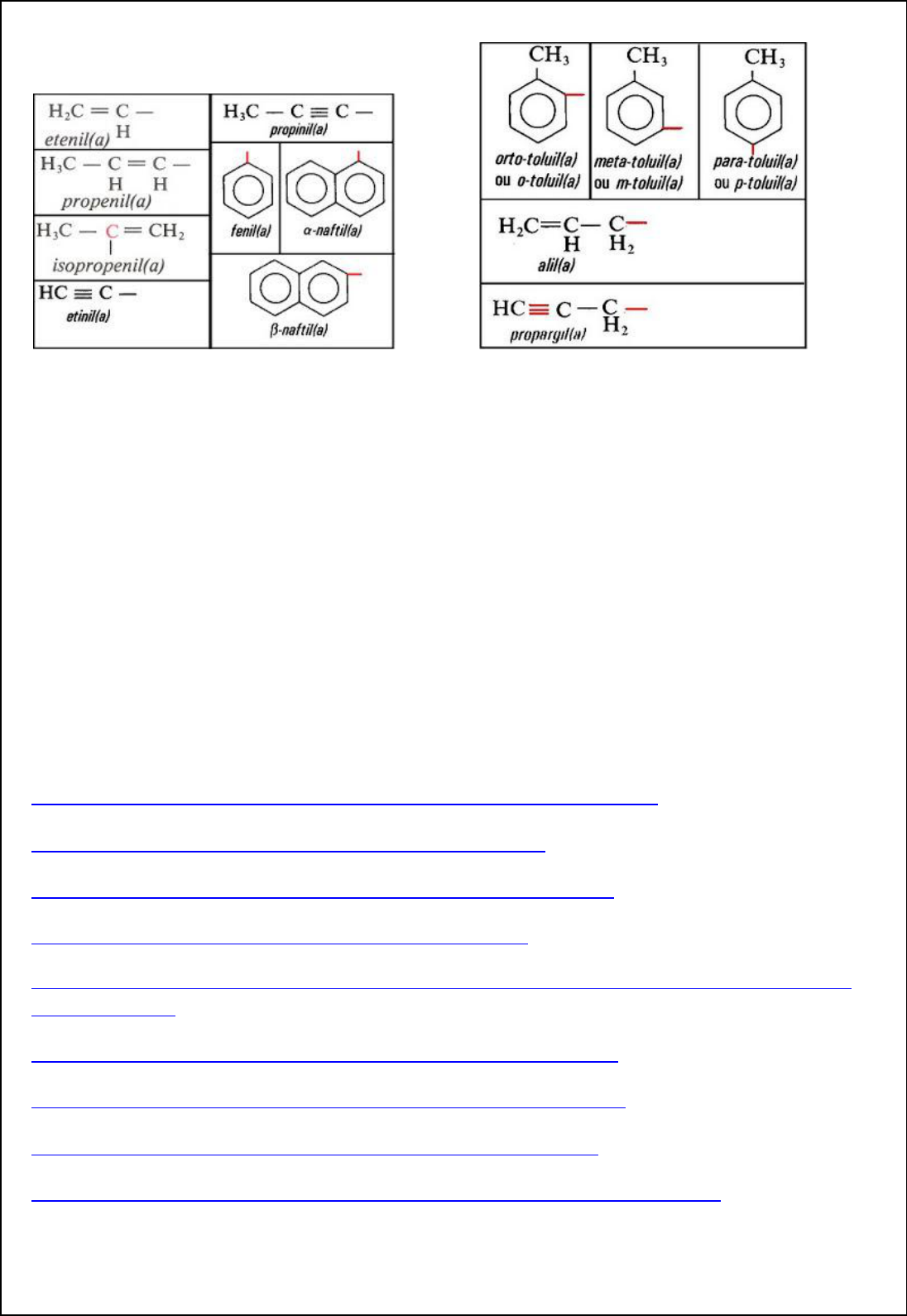
2° N u meração do comp osto
A locali zação das ra mificaçõ es de ve se r i nfor mada pela numeração.
A numeração da cade i a pri nci pal deve segui r a seg ui nte seq ue nci a :
Gr upo f unci o na l > Insat uração > Rami fi cação
Obed ecend o e ste cri tério a numeração da cadei a princi pal deve seg ui r a regra dos menores
números poss ívei s.
Se a cadei a carbôni ca a presentar d uas ou mai s rami fi caçõ es i gua i s, deve m -se usar o s
prefi xos i nd i cadores de q ua nti dade di , tri , tetra , pe nta etc .
Se a ca dei a carbôni ca a presentar d uas ou mai s rami ficaçõe s di ferentes, elas de vem se r
i ndi ca das em ordem alfabé tica.
R eferên cias
ht tps: //a lunoso n li ne. uo l.co m .br /qui mi ca/es tados -fi si cos-da-materia. htm l
ht tps: // www.i nfoescola .com/q ui mica /po ntes -de -hi droge ni o/
ht tps: // www.soq .co m.b r /co nte udo s/em /li ga coesquimi cas/p 5 _2.p hp
ht tps: // ww w. todamateria.com .br /fo rcas -i nte rmolec ulares/
ht tp: //ed uca cao.glo bo .com/q ui mica /ass unto/q ui mi ca -orga ni ca/caracte risticas -dos-compostos -
de-carbono. htm l
ht tps: //a lunoso n li ne. uo l.co m .br /qui mi ca/prop rie dade s -carbono. h tml
ht tps: //m undoed uca cao.bo l. uol.co m.b r /q ui mica/est udo -carbo no. htm
ht tps: //brasi lesco la. uol .com .br/q ui mica / hi b rid i zacao -carbo no. ht m
ht tps: //ma nua ldaqui mica . uol .com.b r/q ui mica -orga ni ca /no menc lat ura-iupac .htm
Prévia do material em texto
UNIVERSIDADE JOSÉ DO ROSÁRIO VELLANO – 2018 Características gerais dos compostos orgânicos Aluna: Gabriela Abrantes Nicácio Matrícula: 202411151 Disciplina: Química Orgânica Belo Horizonte, 05 de outubro de 2018 Características gerais dos compostos orgânicos Forças Intermoleculares na Química Orgânica As forças intermoleculares mantêm duas ou mais moléculas unidas. Estas forças correspondem a ligações químicas capazes unir ou repelir as moléculas de um composto, que podem ser mais ou menos fortes conforme a polaridade das moléculas. As forças intermoleculares geram nos compostos químicos estados físicos diferentes. Existem três tipos de forças intermoleculares, que são: dipolo permanente, dipolo induzido e ligações de hidrogênio. Dipolo permanente Essa força possui intensidade média e ocorre somente em moléculas polares, onde os elétrons estão distribuídos de forma assimétrica, onde uma parte da molécula possui maior densidade eletrônica. Quando a molécula é diatômica, o elemento mais eletronegativo atrai os elétrons da ligação e força um dipolo elétrico. Assim, a parte positiva atrai a parte negativa de outra molécula e assim sucessivamente. Dipolo induzido A força de dipolo induzido é a de menor intensidade e ocorre em moléculas polares e apolares No entanto, quando essas moléculas (ou átomos – gases nobres) se aproximam uma das outras, podem ocorrer deformações nas nuvens eletrônicas, pois há atrações e repulsões entre os elétrons e os núcleos dos átomos. A deformação é apenas temporária, mas forma regiões do átomo ou da molécula que ficam com maior quantidade de elétrons, portanto, são formados dipolos instantâneos. O dipolo instantâneo ao se aproximar de outras moléculas pode induzir a outra molécula a também se polarizar e assim ocorrem forças atrativas - forças de dipolo induzido. Ligações de Hidrogênio A ligação de hidrogênio é a força intermolecular mais intensa, pois existe uma grande diferença de eletronegatividade entre os elementos. Esta ligação ocorre em moléculas polares que têm o hidrogênio unido a elementos com volume atômico baixo e eletronegativos como o hidrogênio, flúor, oxigênio e nitrogênio. De um lado, um átomo muito positivo e, do outro, um átomo muito negativo. Isto faz com que a atração entre estes átomos seja muito forte. Por isso, em geral são sólidos ou líquidos. Entre as moléculas de água ocorre este tipo de força intermolecular. Onde, o oxigênio possui carga parcial negativa e os hidrogênios possuem carga parcial positiva. Então, um hidrogênio de uma molécula é atraído pelo oxigênio de outra molécula e assim por diante, formando ligações de hidrogênio. Uma consequência das pontes de hidrogênio que existem na água é a sua elevada tensão superficial, onde as moléculas que estão no interior do líquido atraem e são atraídas por todas as moléculas vizinhas, de tal modo que as essas forças se equilibram. Já as moléculas da superfície só são atraídas pelas moléculas de baixo e dos lados. Então, essas moléculas se atraem mais fortemente e criam uma película na superfície da água que explica alguns fenômenos, como o fato de alguns insetos caminharem sobre a água, e a forma esférica das gotas de água. Estrutura e Propriedades do átomo de carbono O átomo de carbono O carbono está localizado no grupo 14 (família IVA) e possui seis elétrons, sendo quatro destes localizados em sua camada de valência. Portanto, o carbono é tetravalente e realiza quatro ligações covalentes para adquirir sua estabilidade química. Ele pode realizar ligação com outros átomos de carbono e formar vários tipos de cadeias. O átomo de carbono se liga a elementos comuns em compostos orgânicos, como o hidrogênio, oxigênio, nitrogênio, enxofre e halogênios (Cl, Br, F, I). Estrutura O carbono forma estruturas tetraédricas. Onde o átomo de carbono localiza-se no centro de tetraedros regulares e seus ligantes ocupam as extremidades. As ligações formam entre si ângulos de 109,5º que é a angulação mais estável para estruturas contendo carbono, onde, em cadeias cíclicas, as ligações entre carbonos apresentam ângulos inferiores a 109º5, o que as tornam mais fracas. Tipos de ligação O carbono realiza ligações do tipo covalente com ametais (C, O, S, Cl, Br, I, F, etc.) e hidrogênio. Estas ligações podem ser do tipo σ ou π de acordo com o entrosamento de orbitais na realização da ligação. Quando essas ligações ocorrem por interpenetração de orbitais no mesmo eixo de ligação, a ligação será do tipo σ; quando a ligação for realizada por interação de orbitais paralelos entre si, a ligação realizada será do tipo π. A regra para prever se a ligação do carbono será do tipo σ ou π é: • Ligações simples são do tipo σ; • Em ligações duplas, uma das ligações é do tipo σ e a adicional é do tipo π; • No caso de ligação tripla, uma das ligações é do tipo σ e duas são do tipo π; Hibridização Hibridização é a união de orbitais atômicos incompletos. Um orbital é classificado como incompleto quando ele apresenta apenas um elétron em seu interior ao em vez de dois. A hibridização é um fenômeno natural que ocorre com alguns elementos químicos, como o Fósforo, o Enxofre e o Carbono. A hibridização do Carbono permite que os átomos desse elemento sejam capazes de realizar quatro ligações químicas, com isto, o carbono só realiza quatro ligações após sofrer o fenômeno da hibridização. Classificações do Carbono O carbono pode ser classificado de acordo com o número de ligações que realiza com outros átomos de carbono. As classificações são realizadas da seguinte maneira: • Carbono primário: liga-se a um átomo de carbono; • Carbono secundário: liga-se a dois átomos de carbono; • Carbono terciário: liga-se a três átomos de carbono; • Carbono quaternário: se liga a quatro átomos de carbono. Postulado de Couper-Kekulé Os estudos referentes a estrutura do carbono foram denominados postulados de Couper-Kekulé que estudam o comportamento químico do carbono, eles são subdivididos em três: 1º postulado: Tetravalência constante. O átomo de carbono é tetravalente, essa propriedade permite que esse elemento estabeleça quatro ligações covalentes, onde ele possui dois pares de elétrons disponíveis. 2º postulado: As quatro valências do carbono são iguais. Portanto, um átomo pode se ligar a qualquer um dos quatro carbonos disponíveis que irá formar o mesmo composto. 3º postulado: Encadeamento constante. Átomos de carbono ligam-se diretamente entre si, formando cadeias carbônicas. Essa propriedade também é observada no nitrogênio, enxofre, fósforo e oxigênio. Mas, no carbono essa capacidade de formar quatro ligações é mais pronunciada do que nos outros compostos, por isso é possível observar uma grande variedade de compostos orgânicos e cadeias extensas de carbono. Regras gerais de nomenclatura A nomenclatura IUPAC refere-se ao estabelecimento de regras para a escrita dos nomes dos compostos que são oficialmente aceitos em todo o mundo. Regras: A nomenclatura de Compostos Orgânicos de cadeia normal e não aromáticos segue o seguinte esquema: Prefixo +Infixo + Sufixo Tabela com os respectivos prefixos em relação a quantidade de carbonos presente na cadeia principal: Quantidade de Carbonos Prefixos 1 Met 2 Et 3 Prop 4 But 5 Pent 6 Hex 7 Hept 8 Oct 9 Non 10 Dec 11 Undec 12 Dodec 13 Tridec 14 Tetradec 15 Pentadec 16 Hexadec 17 Heptadec 18 Octadec 19 Nonadec 20 Eicos 21 Honeicos 22 Docos 23 Tricos 24 Tetracos 25 Pentacos 30 Triacont 40 Tetracont 50 Pentacont 60 Hexacont 70 Heptacont Nomenclatura de Compostos com Cadeia Ramificada 1º Escolha da Cadeia Principal A cadeia principal é aquela que apresenta as seguintes características: Possui o grupo funcional; Consta daquela com o maior número possível de insaturações; Possui a sequência mais longa de átomos de carbono ligados entresi. Observações: Caso a cadeia principal ofereça mais de uma possibilidade de escolha, deve-se optar por aquela que fornecer o maior número de ramificações. Quando a cadeia é mista devemos considerar como cadeia principal a cadeia fechada (alicíclica) ou a parte aromática. Ramificações importantes (Radicais): 2° Numeração do composto A localização das ramificações deve ser informada pela numeração. A numeração da cadeia principal deve seguir a seguinte sequencia: Grupo funcional > Insaturação > Ramificação Obedecendo este critério a numeração da cadeia principal deve seguir a regra dos menores números possíveis. Se a cadeia carbônica apresentar duas ou mais ramificações iguais, devem-se usar os prefixos indicadores de quantidade di, tri, tetra, penta etc. Se a cadeia carbônica apresentar duas ou mais ramificações diferentes, elas devem ser indicadas em ordem alfabética. Referências https://alunosonline.uol.com.br/quimica/estados-fisicos-da-materia.html https://www.infoescola.com/quimica/pontes-de-hidrogenio/ https://www.soq.com.br/conteudos/em/ligacoesquimicas/p5_2.php https://www.todamateria.com.br/forcas-intermoleculares/ http://educacao.globo.com/quimica/assunto/quimica-organica/caracteristicas-dos-compostos-de-carbono.html https://alunosonline.uol.com.br/quimica/propriedades-carbono.html https://mundoeducacao.bol.uol.com.br/quimica/estudo-carbono.htm https://brasilescola.uol.com.br/quimica/hibridizacao-carbono.htm https://manualdaquimica.uol.com.br/quimica-organica/nomenclatura-iupac.htm









